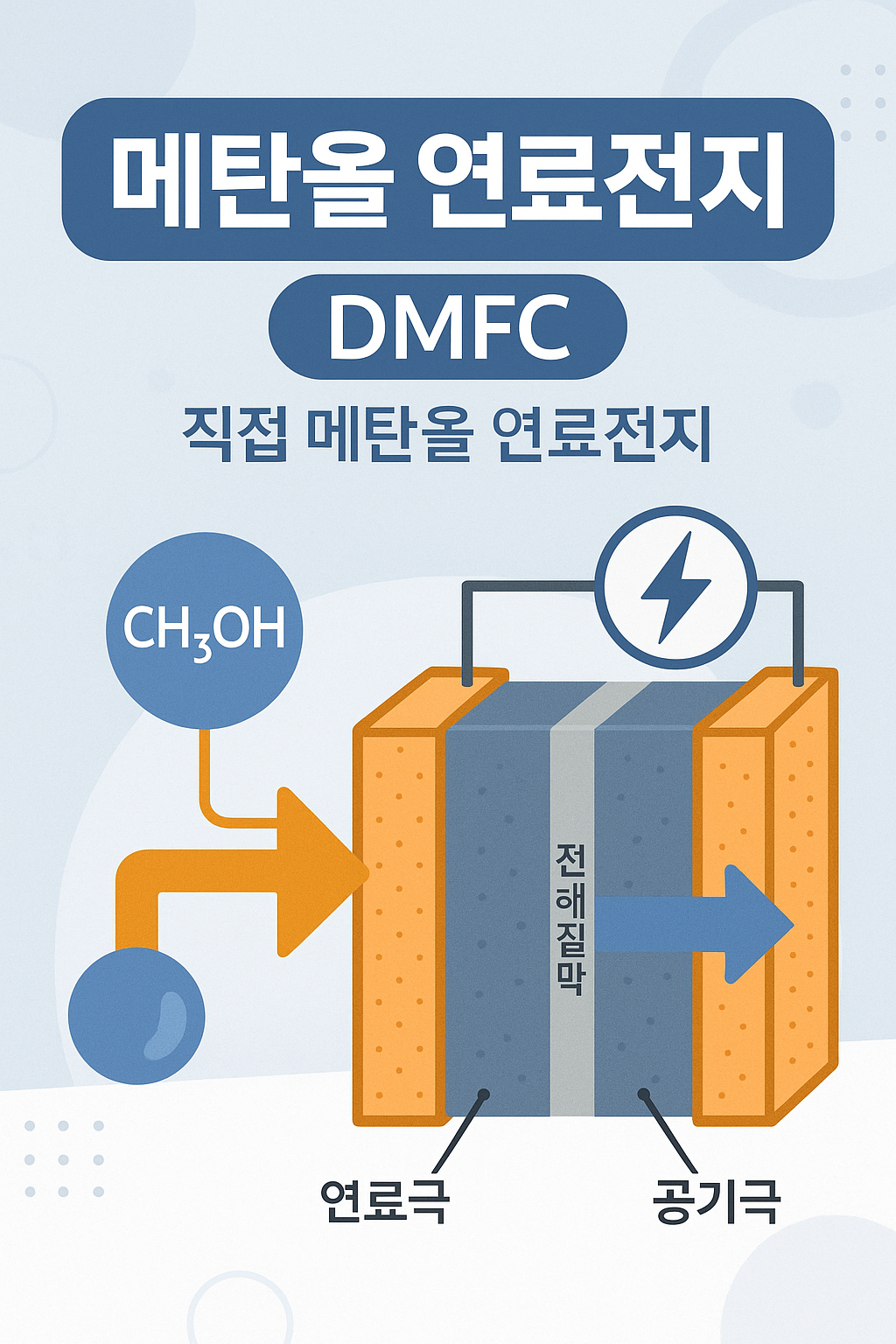
메탄올 연료전지(Direct Methanol Fuel Cell, DMFC)는 액체 연료인 메탄올을 직접 사용하여 전기를 생산하는 연료전지입니다. 이 글에서는 DMFC의 작동 원리, 구조, 장점 및 단점, 그리고 응용 분야에 대해 살펴보겠습니다.
DMFC의 작동 원리
DMFC는 메탄올과 물의 혼합물을 연료로 사용하여 전기를 생성합니다. DMFC의 기본 반응은 다음과 같습니다:
1. 양극(Anode) 반응 :
메탄올과 물이 양극에서 반응하여 이산화탄소, 수소 이온, 그리고 전자를 생성합니다.
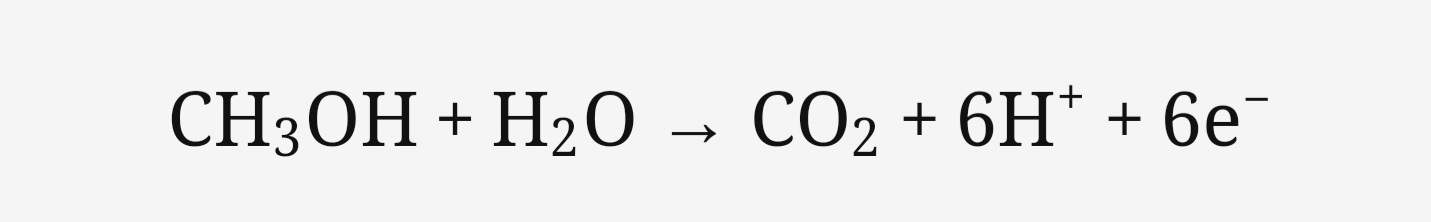
2. 전해질(Electrolyte) :
수소 이온(H+)은 전해질을 통해 음극으로 이동합니다. DMFC에서는 고체 고분자 전해질(PEM)이 주로 사용됩니다.
3. 음극(Cathode) 반응 :
음극에서 수소 이온은 산소와 반응하여 물을 생성하며, 이 과정에서 전자가 필요합니다. 이 전자는 외부 회로를 통해 양극에서 음극으로 이동하며 전류를 생성합니다.
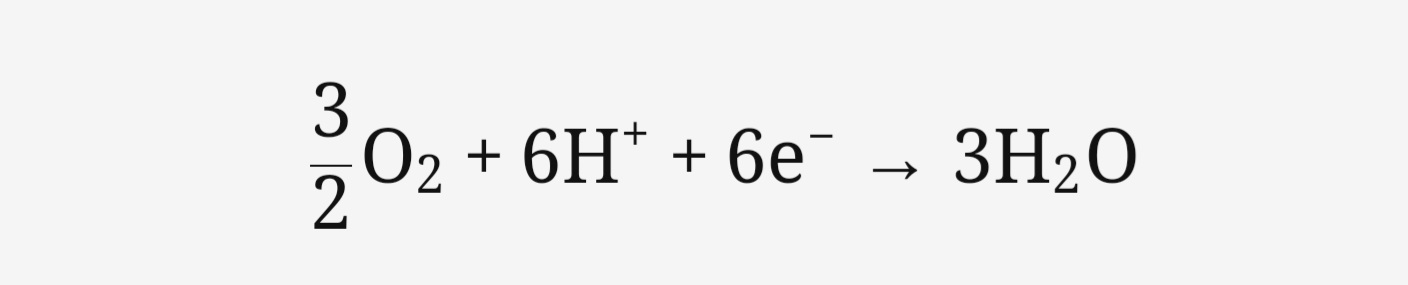
DMFC의 구조
DMFC의 기본 구조는 다음과 같습니다:
- 양극(Anode) : 메탄올 연료가 주입되는 곳으로, 촉매(주로 플라티늄-루테늄)가 메탄올의 산화를 촉진합니다.
- 전해질(Electrolyte) : 수소 이온(H+)만 통과시키는 고체 고분자 전해질막(PEM)이 사용됩니다.
- 음극(Cathode) : 산소(주로 공기 중의 산소)가 공급되며, 촉매(주로 플라티늄)가 산소의 환원을 촉진합니다.
- 가스 확산층(GDL) : 연료와 산화제를 전극에 균일하게 분배하고, 생성된 물을 제거하는 역할을 합니다.
DMFC의 장점 및 단점
장점 :
1. 간편한 연료 저장 : 메탄올은 액체 상태로 저장 및 운반이 용이합니다.
2. 직접 연료 사용 : 메탄올을 직접 사용하므로 복잡한 개질 과정이 필요 없습니다.
3. 고에너지 밀도 : 메탄올은 높은 에너지 밀도를 가지므로 소형 전자기기 등에 적합합니다.
단점 :
1. 낮은 효율 : 다른 연료전지에 비해 효율이 낮은 편입니다.
2. 촉매 중독 : 메탄올의 분해 과정에서 생성된 일산화탄소가 촉매를 중독시켜 성능 저하를 초래할 수 있습니다.
3. 연료 교차오염 : 전해질막을 통해 메탄올이 음극으로 이동하는 크로스오버 현상이 발생할 수 있습니다.
DMFC의 응용 분야
DMFC는 그 특성 덕분에 여러 분야에서 사용되고 있습니다:
1. 휴대용 전자기기 :
- 노트북, 스마트폰, 태블릿 등의 소형 전자기기에서 장시간 전력 공급이 필요할 때 사용됩니다.
2. 군사 및 야외 활동 :
- 배터리 대체 용도로, 장시간 지속적인 전력 공급이 필요한 군사 장비와 야외 활동 장비에 사용됩니다.
3. 소형 이동 수단 :
- 전기 자전거나 소형 전기 스쿠터 등에서 사용될 수 있습니다.
메탄올 연료전지(DMFC)는 액체 연료인 메탄올을 사용하여 전기를 생산하는 연료전지로, 간편한 연료 저장과 높은 에너지 밀도 덕분에 다양한 응용 분야에서 활용되고 있습니다. 휴대용 전자기기, 군사 및 야외 활동 장비, 소형 이동 수단 등에서 DMFC의 잠재력은 매우 큽니다. 기술적 단점들을 극복하기 위한 지속적인 연구와 발전을 통해 DMFC의 효율성과 안정성을 향상시켜 더 많은 분야에서 활용될 수 있기를 기대합니다.